東方生物的呼吸道三聯(lián)檢試劑 成為全球首款取得美國(guó)FDA De Novo認(rèn)證的產(chǎn)品
繼浙江東方基因生物制品股份有限公司下屬子公司美國(guó)衡健生物科技有限公司的Healgen COVID-19/Flu A&B Ag Combo Rapid Test Cassette (Swab)(Healgen新冠、甲乙流抗原快速聯(lián)合檢測(cè)試劑(鼻拭子))于2024年6月取得了美國(guó)U.S. Food & Drug Administration(美國(guó)食品藥品監(jiān)督管理局,簡(jiǎn)稱“FDA”)批準(zhǔn)的緊急使用授權(quán)(EUA)。
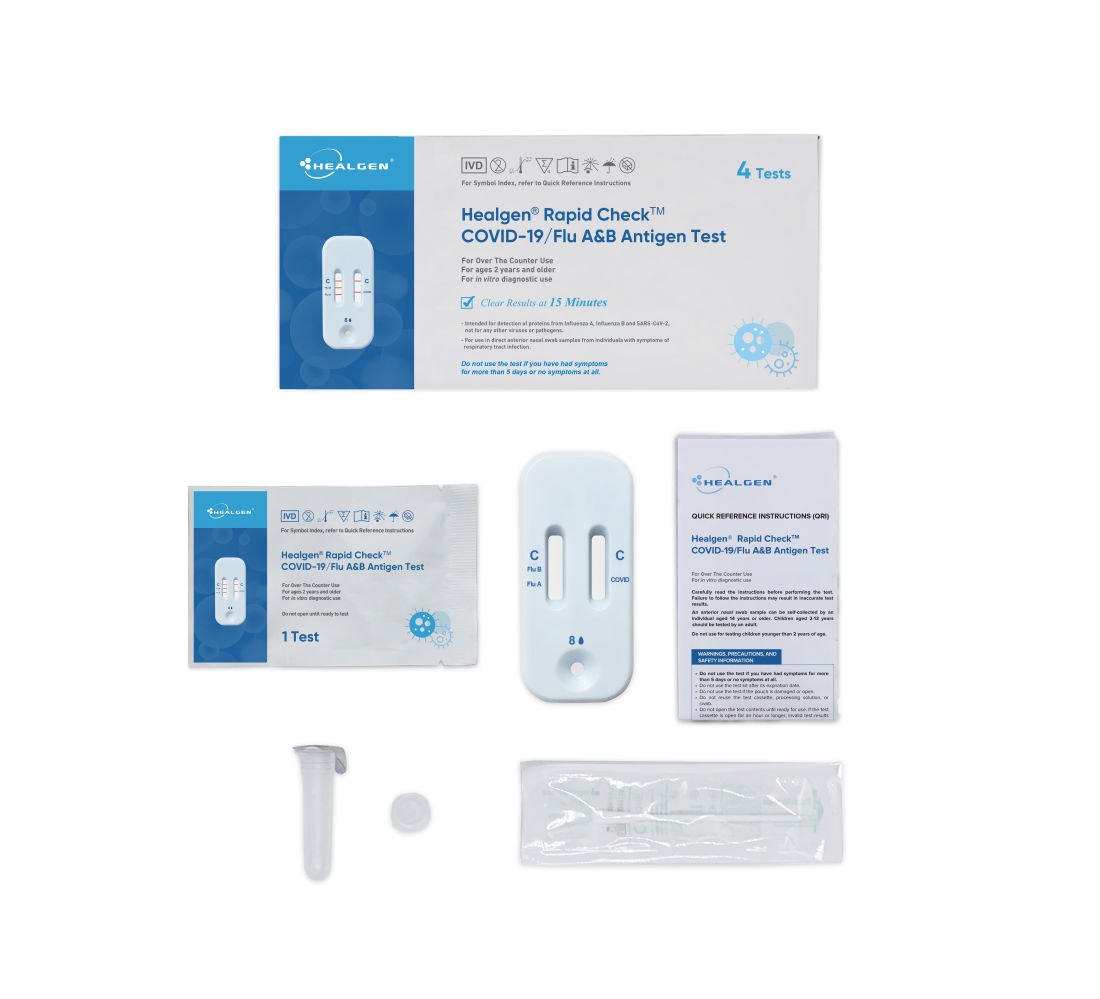
近日,美國(guó)FDA官網(wǎng)又發(fā)布了《FDA授權(quán)在緊急使用授權(quán)之外的首款流感和新冠病毒聯(lián)合家用檢測(cè)試劑》的新聞,以及根據(jù)東方生物發(fā)布的最新公告,美國(guó)衡健的Healgen Rapid Check COVID-19/flu A&B Antigen Test(Healgen新冠、甲乙流抗原快速聯(lián)合檢測(cè)試劑)于美國(guó)時(shí)間2024年10月7日進(jìn)一步取得美國(guó)FDA批準(zhǔn)De Novo認(rèn)證,這款產(chǎn)品應(yīng)用橫向流動(dòng)免疫層析法,適用于有呼吸道感染體征和癥狀的個(gè)體的前鼻拭子樣本中抗原檢測(cè),檢測(cè)來自于SARS-CoV-2病毒核衣殼抗原以及甲型和乙型流感病毒的核蛋白抗原,在約15分鐘內(nèi)快速定性、鑒別檢測(cè)新型冠狀病毒或甲/乙型流感病毒感染的檢測(cè)結(jié)果,作為全球首款取得美國(guó)FDA De Novo 認(rèn)證的產(chǎn)品,也是在美國(guó)地區(qū)首款獲得FDA De Novo認(rèn)證的非處方(OTC)檢測(cè)產(chǎn)品,通過傳統(tǒng)的上市前審查途徑獲得上市許可,能夠滿足在非緊急使用受權(quán)情況下的使用,可由非專業(yè)用戶在家庭自測(cè)使用。目前,其他公司的非處方流感/新冠檢測(cè)在緊急使用授權(quán)下可用。
該試劑可供14歲或以上的個(gè)人自行采集樣本進(jìn)行檢測(cè),或成年人對(duì)2歲及2歲以上的人采集樣本檢測(cè)。數(shù)據(jù)顯示,該檢測(cè)試劑可分別正確識(shí)別99%的SARS-CoV-2陰性樣本和92%的陽(yáng)性樣本;99.9%的甲型流感和乙型流感陰性樣本,92.5%甲型流感和90.5%乙型流感的陽(yáng)性樣本。該檢測(cè)試劑的驗(yàn)證數(shù)據(jù)來自于美國(guó)國(guó)立衛(wèi)生研究院(NIH)與FDA自2021年開始聯(lián)合啟動(dòng)的快速加速診斷技術(shù)項(xiàng)目(RADx?) 中的獨(dú)立測(cè)試評(píng)估項(xiàng)目(ITAP),該項(xiàng)目旨在加速測(cè)試評(píng)估以支持FDA的監(jiān)管審查,并向公眾提供高質(zhì)量、準(zhǔn)確和可靠的診斷測(cè)試。
“隨著進(jìn)入今年的流感季節(jié),許多人都在腦海中浮現(xiàn)出 COVID-19等呼吸道疾病,有效檢測(cè)這些病原體的能力可能會(huì)對(duì)我們的日常生活產(chǎn)生影響。今天的授權(quán)擴(kuò)大了有呼吸道癥狀的個(gè)人在舒適的家中獲得健康信息的選擇范圍,”FDA器械和放射衛(wèi)生中心代理主任、醫(yī)學(xué)博士米歇爾·塔弗表示:“FDA繼續(xù)采取行動(dòng),支持開發(fā)和提供用于多種疾病的家庭檢測(cè)。”
本次東方生物子公司美國(guó)衡健的Healgen新冠、甲乙流抗原快速聯(lián)合檢測(cè)試劑取得美國(guó)FDA De Novo認(rèn)證,順利完成了從專業(yè)版到家庭自測(cè)版的布局,同時(shí)作為全球第一家在美國(guó)完成從緊急使用授權(quán)到非緊急使用授權(quán)(即可長(zhǎng)期使用)布局的企業(yè),標(biāo)志著東方生物呼吸道聯(lián)合檢測(cè)產(chǎn)品在美國(guó)地區(qū)取得了重要的實(shí)質(zhì)性進(jìn)展,進(jìn)一步增強(qiáng)了公司在美國(guó)地區(qū)呼吸道聯(lián)合檢測(cè)應(yīng)用領(lǐng)域的核心競(jìng)爭(zhēng)力,有利于美國(guó)市場(chǎng)的整體拓展和品牌影響力。
東方生物表示,公司會(huì)持續(xù)關(guān)注美國(guó)市場(chǎng)對(duì)上市產(chǎn)品的實(shí)際檢測(cè)需求動(dòng)態(tài),積極推動(dòng)本產(chǎn)品的市場(chǎng)推廣銷售。一鳴
原文鏈接:FDA Authorizes Marketing of First Home Flu and COVID-19 Combination Test Outside of Emergency Use Authorities | FDA https://www.fda.gov/news-events/press-announcements/fda-authorizes-marketing-first-home-flu-and-covid-19-combination-test-outside-emergency-use
- 免責(zé)聲明:本文內(nèi)容與數(shù)據(jù)僅供參考,不構(gòu)成投資建議。據(jù)此操作,風(fēng)險(xiǎn)自擔(dān)。
- 版權(quán)聲明:凡文章來源為“大眾證券報(bào)”的稿件,均為大眾證券報(bào)獨(dú)家版權(quán)所有,未經(jīng)許可不得轉(zhuǎn)載或鏡像;授權(quán)轉(zhuǎn)載必須注明來源為“大眾證券報(bào)”。
- 廣告/合作熱線:025-86256149
- 舉報(bào)/服務(wù)熱線:025-86256144

